I moderni programmi di farmacovigilanza documentano con sempre maggiore frequenza nuovi principi attivi in grado di alterare il parodonto profondo e superficiale.
La capillare e crescente diffusione dei farmaci antiepilettici è principale conseguenza dei sempre più affinati metodi diagnostici dell’epilessia, il loro utilizzo in passato era solo connesso alla patologia principale per cui erano prescritti, attualmente questi farmaci vengono ampiamente utilizzati anche come stabilizzatori dell’umore.
Tra i farmaci noti per la complessa gestione parodontale del paziente derivante dagli effetti di alterazione sito specifica, si denota il vasto gruppo degli Antiepilettici o Anticonvulsivanti.
Sempre più frequentemente i pazienti, a cui vengono prescritti questi farmaci, presentano alterazioni del parodonto superficiale. Il grado di alterazione e la stessa probabilità che tale alterazione si verifichi realmente sono spesso mediati da polimorfismi genetici del paziente, condizioni sistemiche basali e dosaggio del farmaco.
Considerati dei reali salvavita, i principi attivi sviluppati negli ultimi due secoli, si sono ampiamente diffusi nella popolazione affetta dalle numerose forme cliniche di sindromi e crisi epilettiche poiché in grado di determinare una adeguata qualità della vita. Sovente è necessario proseguire l’assunzione per l’intera vita del paziente.
Tali condizioni pongono il professionista odontoiatrico nella reale necessità di conoscere la farmacoterapia del paziente epilettico e i molteplici connessi effetti di alterazione parodontale, spesso cronicizzata dai lunghi periodi di assunzione, che la letteratura ha diffusamente riportato negli ultimi decenni.
Il background patologico orale conseguente all’assunzione di molti farmaci anticonvulsivanti si compone principalmente di fenomeni edemigeni marginali del parodonto superficiale, eritemi, pseudo tasche e alterate risposte immunitarie/flogistiche. La complessa detergibilità e la difficoltà di accesso strumentale igienico causato dal tessuto gengivale marginale alterato ipertrofico/iperplastico può indurre fenomeni parodontopatogeni cronicizzati e deperimenti conservativi conducendo alla perdita dell’elemento con gravi ripercussioni sullo stato di salute orale del paziente. I tessuti orali alterati possono inoltre interporsi nel corso della fonazione e alimentazione inducendo costanti flogosi settoriali ad ingravescenza progressiva.
I documentati casi clinici di alterazione parodontale da antiepilettici impongono al professionista odontoiatrico la conoscenza dei meccanismi etiopatogenetici, dei linkage clinici tra assunzione farmacologica ed effetti patologici obiettivabili, la gestione igienica parodontale mediante terapia causale e le particolari eventualità che implicano il ricorso a tecniche chirurgiche resettive. La knowledge clinica è base fondamentale per la corretta gestione in office e in home del paziente, spesso impossibilitato ad interrompere l’assunzione del principio attivo. Il sinergico team work con i clinici neurologi risulta fondamentale per limitare i secondarismi delle terapie anche in fasi precedenti all’inizio del trattamento.
Overview del paziente epilettico e suo trattamento farmacologico.
Al 2017 si riconoscono almeno 9 gruppi principali di crisi ed eventi epilettici secondo l’ILAE (international league against epilepsy).
Crisi generalizzata tonico-clonica
Crisi generalizzata di assenza
Crisi generalizzata mioclonica
Crisi generalizzata atonica
Crisi epilettiche focali
Crisi parziale semplice senza alterazione della coscienza.
Crisi parziale completa con alterazione della coscienza.
Crisi parziale con generalizzazione secondaria.
Spasmi epilettici.
L’epilessia è una condizione neurologica cronica o acuta (transitoria) caratterizzata da convulsioni, manifestazioni neurologiche e/o muscolari spesso associate all’alterazione dello stato di coscienza.
La patogenesi è multifattoriale ed è attribuibile a condizioni genetiche, tossicologiche, traumatismi e come conseguenza di malformazioni causate da sindromi (es. Sindrome di Stürge Weber). Alcune forme possono altresì essere acquisite da altre condizioni cliniche in grado di alterare il decorso neuro/vascolare encefalico.
La pericolosità dei fenomeni epilettici risiede nella sospensione della respirazione osservata nel corso dell’attacco convulsivo, nei traumatismi eventualmente riportabili in seguito ad accidentali cadute o ferite causate da involontari interposizioni della lingua tra le arcate dentarie, sostenuti dal trisma bilaterale dei muscoli massetteri.
L’epilessia conta, solo in Italia, circa 500.000 persone affette e 30.000 nuovi casi per anno, con incidenza più elevata nei bambini e negli anziani. In Europa circa 6 milioni di persone presentano una forma di epilessia in fase attiva (cioè con crisi persistenti e/o tuttora in trattamento).
L’epilessia interessa globalmente circa l’1% della popolazione e la sua prevalenza, nella maggior parte dei paesi sviluppati, oscilla tra lo 0,5 e l’1% della popolazione, con picchi di maggior incidenza nei bambini e nella terza età. (LICE).
Nelle forme non-farmacoresistenti, i farmaci antiepilettici sono utilizzati allo scopo di sedare le convulsioni. Le crisi possono presentare effetti secondari anche gravi dovuti all’alterato stato di coscienza scaturibile dal singolo evento o da un gruppo di eventi epilettici (clusters o crisi a grappolo).
Principali molecole in grado di causare alterazione parodontale.
L’uso della farmacoterapia per il contenimento delle crisi epilettiche, risale agli inizi del ventesimo secolo. Le associazioni con l’aumento di volume gengivale e possibili meccanismi, sono stati chiarificati (sebbene solo parzialmente) in seguito, dopo il 1975.
Nonostante l’estesa quantità di molecole disponibili per il trattamento del paziente epilettico, le revisioni aggiornate attribuiscono ruoli di patogenicità diretta per il parodonto superficiale ad alcune specifiche categorie.
-Fenitoina (difenilidantoina): I suoi effetti sul paziente epilettico sono studiati e monitorati dal 1938. E’ uno fra i più antichi farmaci disponibili per il trattamento.
L’assunzione orale induce aumento di volume gengivale marginale. Tali effetti sono stati riscontrati in pazienti edentuli riscontrando che i possibili meccanismi etio patologici della formazione edemigena non siano da attribuire unicamente all’alterata risposta dei tessuti a stimoli chimici/batterici esterni ma a cause intrinseche al tessuto stesso.
L’alterata crescita gengivale induce la formazione di nicchie ritentive che facilitano la progressiva sedimentazione di depositi alimentari e di colonie batteriche. La formazione di depositi di placca e la complessità detersiva esacerbano progressivamente l’edema marginale.
-Sodio Valproato: Farmaco utilizzato prettamente nella gestione delle crisi epilettiche entro i 15/16 anni. Raramente è utilizzato nell’adulto.
Clinicamente si riscontrano edemi marginali simil-fenitoina. Le alterazioni possono avere inizio anche a 18 mesi dall’inizio della terapia e risolversi entro i 3 mesi dopo la sospensione del farmaco.
Le alterazioni indotte da sodio valproato sono spesso associate a iper sensibilità farmaco-specifiche, a differenza di quanto riscontrato nelle altre categorie di molecole per il trattamento dell’epilessia, in grado di alterare direttamente meccanismi di replicazione cellulare e/o formazione di matrice extracellulare marginale.
-Fenobarbitone: I casi riportati in letteratura pongono attenzione su caratteri comuni delle alterazioni gengivali riscontrate in pazienti in terapia con Fenobarbitone:
-Le alterazioni di volume marginali presentano forma lobulata;-L’aumento di volume coinvolge prettamente le regioni marginali degli elementi posteriori
-Si assiste generalmente ad una graduale regressione dei secondarismi ipertrofici/iperplastici dopo shaping chirurgico della gengiva e progressiva ripresa di una adeguata detergibilità.
-Vigabatrin: E’ una molecola relativamente recente. I casi riportati in letteratura non discernono in modo consensuale sulla reale natura delle alterazioni gengivali farmaco indotte. L’etio-patogenesi potrebbe essere attribuita a meccanismi di iper sensibilità individuale specifica.
Le lesioni generate a livello superficiale sono raramente stabilizzate con terapia causale che si rivela tanto più inefficace quanto tardivamente attuata.
Le alterazioni sono riscontrate già a due mesi dall’inizio della terapia e trovano, nei casi più gravi, naturale risoluzione nella terapia di shaping chirurgico.
Meccanismi etio patogenetici.
Sebbene non completamente chiarificato, il meccanismo etiopatogenetico delle alterazioni di volume gengivale è stato ampiamente monitorato in studi clinici in vivo e in vitro.
Il primo caso di alterazione gengivale indotta da farmaci epilettici è stato riscontrato da Kimball nel 1939 in un paziente in trattamento con Fenitoina.
I linkage clinici ipotizzati sono stati analizzati in letteratura dalla seconda metà del ‘900.
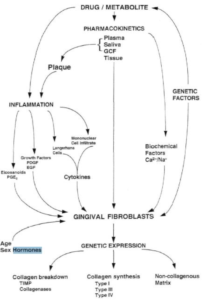
Nel 1996 Seymour e coll. hanno proposto il modello multifattoriale nell’importante lavoro “The pathogenesis of drug-induced gingival overgrowth” .
Le alterazioni del parodonto superficiale sarebbero conseguenza di un complesso insieme di cause direttamente connesse all’assunzione del farmaco anti epilettico ed esacerbate dalle complessità igieniche successivamente riscontrate dal paziente per complicata detergibilità:
-interazioni dei farmaci con la replicazione dei fibroblasti;
-età;
-sesso;
-alterazioni della matrice extracellulare;
I meccanismi non-infiammatori proposti includono:
-Difettosa attività delle collagenasi di matrice a causa della riduzione dell’assorbimento di acido folico;
-Sovra-espressione di glicosaminoglicani nella matrice extra cellulare;
-Blocco della sintesi di aldosterone nella corteccia surrenale e conseguente aumento di feedback del livello di ormone adrenocorticotropo;
-Iper-espressione del fattore di crescita dei cheratinociti (KGF);
-Iper espressione genetica e conseguente aumento della sintesi del recettore di membrana EGF (epithelial growth factor).
In alternativa, l’infiammazione può svilupparsi come
risultato di effetti tossici diretti del farmaco concentrato nel liquido crevicolare del solco marginale. L’indotta risposta potrebbe condurre alla sovra-regolazione di diverse citochine come il Transforming Growth Factor – TGF-β:
-Aumento di infiltrato di cellule di Langherans nell’epitelio gengivale;
-Risposta selettiva di Linfociti T in tessuti gengivali interessati da aumento di volume gengivale: la complessa rete multifattoriale in grado di determinare alterazione parodontale superficiale, potrebbe essere regolata da sub-popolazioni di Linfociti T, ampiamente reperiti in valutazioni istologiche di pazienti in cura con fenitoina.
-Sovra espressione di citochine indotta dall’incremento di popolazione di cheratinociti.
Management terapeutico: Il ruolo sinergico del team odontoiatrico nella prevenzione delle alterazioni farmaco indotte.
Il management terapeutico dell’ipertrofia/iperplasia gengivale in pazienti trattati con ciclosporina, data l’etiologia multifattoriale delle lesioni, è di complessa strutturazione e deve essere affrontato compatibilmente con le condizioni sistemiche del paziente, il dosaggio, i tempi di somministrazione del farmaco e la gravità delle lesioni orali.
Prevenzione
Una severa e puntuale attività di prevenzione dovrebbe sempre essere proposta prima dell’inizio della terapia con antiepilettici.
Il paziente epilettico dovrebbe essere sottoposto ad un’accurata ispezione del cavo orale per la rilevazione delle capacità igienico/detersive, la focalizzazione istruttivo/motivazionale sulle aree a maggior rischio di deposito di placca e l’eliminazione di fattori irritanti. Il controllo del biofilm può mitigare in modo sensibilmente importante il decorso delle lesioni, favorendo lo sviluppo di formazioni a dimensione più contenuta ma non potrebbe prevenire in modo assoluto la loro comparsa.
L’accesso del paziente in trattamento farmacologico alle cure odontoiatriche avviene prevalentemente a terapia avviata ed è estremamente frequente la necessitò di stabilizzare quadri patologici di alterazione marginale del volume gengivale in stato avanzato. Le terapie fondano la loro efficacia sulla necessità di ridurre il deposito batterico in grado di indurre risposta infiammatoria nelle nicchie ritentive coronali subgengivali e/o la loro rimozione mediante shaping chirurgico.
L’igienista dentale e l’odontoiatra dovrebbero svolgere ruolo di management coordinato nel controllo e nella rivalutazione bimestrale del paziente. Il controllo igienico efficace potrebbe compensare in modo valido l’alterazione infiammatoria, determinandone la regressione integrale o parziale. Controlli puntuali mirano alla selezione di scelte terapeutiche più efficaci, non esclusa la terapia chirurgica e la discussione del piano di cure con il team neurologico.
Terapia chirurgica e igienica
La terapia causale igienica si dimostra vincente nel contenimento flogistico delle formazioni ipertrofiche/iperplastiche nel paziente epilettico.
La complessità strumentale è insita nella formazioni di pseudotasche in cui il tessuto occupa una vasta area della superficie coronale e radicolare del dente, rendendo spesso impossibile la strutturazione di manovre igieniche domiciliari. Il controllo di tali condizioni dovrebbe essere strutturato tri o quadrimestralmente, associando rimozione dei depositi di tartaro a minima traumaticità e un’attenta mitigazione del biofilm batterico.
Nell’impossibilità di procedere a tali azioni per la massiva presenza di tessuto ipertrofico, è spesso suggerita un’ibridazione con la terapia non chirurgica a ridotta invasività, nell’intento di escidere le aree tissutali in eccesso e favorire i processi di detersione domiciliare e professionale.
Le ragioni del trattamento chirurgico sono spesso associate a motivazioni meramente estetiche e sembrano essere indicate in lesioni che non rispondano a terapie farmacologiche e causali, stabilizzate da tempo a livello vestibolare e coprenti oltre i due terzi della corona dentale. La tecnica prescelta per l’escissione dovrebbe sempre essere selezionata per la minor invasività, la più contenuta traumaticità post operatoria, ridotte tempistiche di guarigione e le maggiori possibilità di restitutio ad integrum. Il chirurgo dovrebbe costantemente essere aggiornato sulla terapia del paziente epilettico ed eventuali modifiche di dosaggio e/o principio attivo.
Conclusioni:
L’accesso del paziente alla cure più recenti e la diffusione di una sempre più puntuale cultura della salute orale, aumenta la probabilità che il professionista odontoiatrico si interfacci con il paziente epilettico in farmacoterapia avanzata.
Risulta fondamentale, quindi, l’approfondita conoscenza dei meccanismi etio patogenetici alla base delle più comuni alterazioni orali indotte dai farmaci e la conoscenza della loro farmacodinamica. Tali prerogative rendono possibile la puntuale valutazione della gravità delle condizioni cliniche orali del paziente e l’agevole strutturazione di piani di richiamo. Risulta focale il contenimento dei secondarismi gengivali delle terapie farmacologiche con interventi di incremento della adherence domiciliare e/o la gestione chirurgica delle gravi ipetrofie/iperplasie.
L’approfondita conoscenza degli effetti secondari della terapia anti convulsivante, dovrebbe rendere possibile il quotidiano interfacciamento del professionista odontoiatrico con il care team neurologico del paziente epilettico. La costituzione di un work team operativo multidisciplinare si pone nell’ottica di un globale e costante controllo sistemico che ponga le sue basi anche sulla valutazione dei tessuti orali e si traduca nella migliore scelta terapeutica possibile per il paziente.
Full text e bibliografia disponibile a richiesta
Autore articolo Dott. M. Fanuli